Trong thế giới vi mô đầy kỳ diệu, các phân tử không tồn tại một cách đơn lẻ. Chúng liên tục tương tác với nhau thông qua những lực liên kết đặc biệt, quyết định tính chất của mọi vật chất xung quanh ta. Bài viết này sẽ cùng bạn khám phá hai loại liên kết yếu nhưng vô cùng quan trọng: liên kết hydro và tương tác Van der Waals, những “chất keo” vô hình giúp giải thích vô số hiện tượng tự nhiên thú vị.
Nếu bạn đang tìm kiếm một lộ trình bài bản để xây dựng nền tảng Hóa học vững chắc, từ những khái niệm cơ bản nhất như liên kết phân tử, hãy tham khảo bài viết Từ Mất Gốc Đến Giỏi Hóa: Bí Quyết Lấy Lại Căn Bản và Chinh Phục Môn Học “Khó Nhằn”. Nó sẽ là bước đệm hoàn hảo trước khi đi sâu vào những chủ đề phức tạp hơn.
Liên Kết Hydro: Sức Mạnh Của Những “Cầu Nối” Yếu
Liên kết hydro không phải là một liên kết hóa học mạnh như liên kết cộng hóa trị hay liên kết ion. Nó là một liên kết yếu được hình thành giữa một nguyên tử hydro (đã liên kết cộng hóa trị với một nguyên tử có độ âm điện lớn như Flo, Oxi hay Nitơ) và một cặp electron chưa liên kết (cặp electron tự do) của một nguyên tử có độ âm điện lớn khác thuộc về một phân tử lân cận.

Hãy lấy nước (H₂O) làm ví dụ điển hình. Nguyên tử oxy có độ âm điện lớn, kéo cặp electron dùng chung trong liên kết O-H về phía mình, khiến nguyên tử hydro mang một phần điện tích dương (δ+). Phần điện tích dương này sẽ hút cặp electron chưa liên kết (mang điện tích âm δ-) của nguyên tử oxy thuộc một phân tử nước khác. Lực hút tĩnh điện này chính là liên kết hydro, thường được biểu diễn bằng ba chấm (…).
So Sánh Sức Mạnh Các Loại Liên Kết
Nếu xếp theo độ mạnh giảm dần, chúng ta có:
– Liên kết ion: Mạnh nhất.
– Liên kết cộng hóa trị: Mạnh.
– Liên kết hydro: Yếu.
– Tương tác Van der Waals: Yếu nhất.
Điều này cho thấy liên kết hydro tuy yếu hơn liên kết hóa học thông thường, nhưng lại mạnh hơn đáng kể so với các tương tác vật lý khác giữa các phân tử.
Vai Trò Và Ảnh Hưởng Của Liên Kết Hydro
Sự hiện diện của liên kết hydro tạo nên những tính chất đặc biệt cho các hợp chất, đặc biệt là nước:
- Nhiệt độ sôi và nhiệt độ nóng chảy cao: So với các hợp chất có khối lượng phân tử tương tự như H₂S, H₂Se, nước (H₂O) có nhiệt độ sôi (100°C) và nóng chảy cao bất thường. Đó là vì cần cung cấp thêm năng lượng để phá vỡ mạng lưới liên kết hydro giữa các phân tử nước trước khi chúng có thể chuyển sang trạng thái khí hoặc lỏng.
- Tính tan tốt: Nước là một dung môi tuyệt vời, không chỉ hòa tan các chất ion mà còn hòa tan nhiều hợp chất cộng hóa trị phân cực, đặc biệt là những chất có khả năng tạo liên kết hydro với nước. Ví dụ, ethanol (C₂H₅OH) tan vô hạn trong nước nhờ nhóm -OH của nó có thể tạo liên kết hydro với phân tử nước.

- Hiện tượng nước đá nổi: Khi đóng băng, các phân tử nước sắp xếp thành một cấu trúc tinh thể mạng lưới rỗng, với mỗi phân tử liên kết hydro với 4 phân tử lân cận. Cấu trúc này khiến thể tích nước đá lớn hơn thể tích nước lỏng tương ứng, làm mật độ giảm và nước đá nổi lên. Đây cũng là lý do chúng ta không nên để chai nước, lon nước ngọt đầy trong ngăn đá – khi đóng băng, thể tích tăng lên có thể làm vỡ chai/lon.
- Sức căng bề mặt: Liên kết hydro giữa các phân tử nước ở bề mặt và lớp nước bên dưới tạo ra một “màng” co giãn, gọi là sức căng bề mặt. Điều này giải thích tại sao một số loài côn trùng nhẹ như con nhện nước có thể dễ dàng di chuyển trên mặt nước mà không bị chìm.
Tương Tác Van Der Waals: Lực Hút Từ Những “Lưỡng Cực Thoáng Qua”
Nếu liên kết hydro chỉ xuất hiện ở những phân tử có nguyên tử H liên kết với F, O, N, thì tương tác Van der Waals là lực phổ biến hơn, xuất hiện ở hầu hết các phân tử, kể cả phân tử không phân cực.
Lưỡng Cực Tạm Thời và Lưỡng Cực Cảm Ứng
Tương tác này được hình thành từ hai hiện tượng:
1. Lưỡng cực tạm thời: Trong một phân tử, sự chuyển động của các electron có thể tập trung tạm thời về một phía, tạo ra một đầu tích điện âm và một đầu tích điện dương trong chốc lát. Đây gọi là lưỡng cực tạm thời.
2. Lưỡng cực cảm ứng: Lưỡng cực tạm thời của phân tử này có thể làm phân cực phân tử lân cận, cảm ứng tạo ra một lưỡng cực tương ứng trên phân tử đó.

Lực hút tĩnh điện yếu giữa các lưỡng cực tạm thời và lưỡng cực cảm ứng này chính là tương tác Van der Waals. Nó giúp các phân tử tập hợp lại với nhau, tạo thành một mạng lưới tương tác yếu.
Ảnh Hưởng Đến Tính Chất Vật Lý
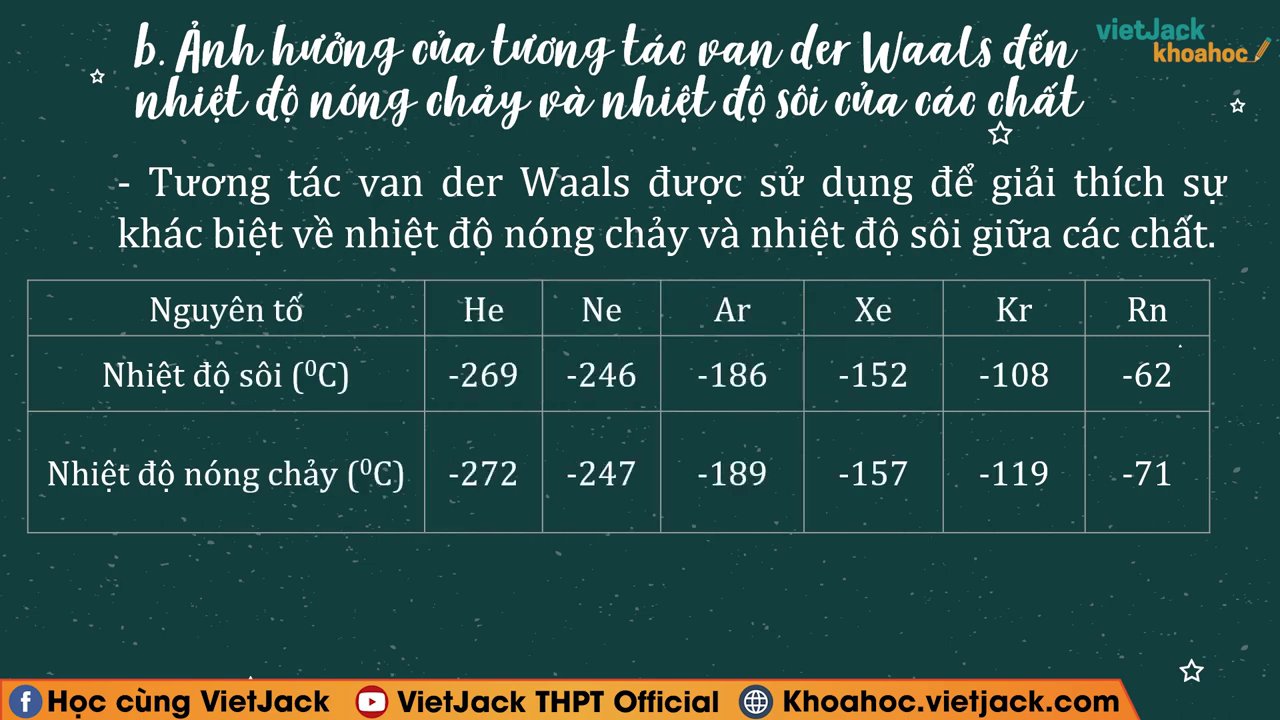
Tương tác Van der Waals thường được dùng để giải thích sự khác biệt về nhiệt độ sôi và nhiệt độ nóng chảy giữa các chất, đặc biệt là trong cùng một nhóm hợp chất.
- Khối lượng và kích thước phân tử: Khi khối lượng phân tử tăng, kích thước phân tử tăng, số electron nhiều hơn dễ tạo ra lưỡng cực tạm thời mạnh hơn. Do đó, tương tác Van der Waals càng mạnh, đòi hỏi nhiều năng lượng hơn để phá vỡ, dẫn đến nhiệt độ sôi và nhiệt độ nóng chảy tăng. Ví dụ, trong dãy khí hiếm (He, Ne, Ar, Kr, Xe) hay dãy halogen (F₂, Cl₂, Br₂, I₂), nhiệt độ sôi tăng dần theo chiều tăng của khối lượng phân tử.
Tóm lại, chúng ta có thể rút ra hai kết luận chính về tương tác Van der Waals:
1. Đây là lực tương tác yếu nhất giữa các phân tử, hình thành do sự xuất hiện của các lưỡng cực tạm thời và lưỡng cực cảm ứng.
2. Tương tác này làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của chất. Nó càng mạnh khi khối lượng và kích thước phân tử càng lớn.
Bài Tập Vận Dụng: Củng Cố Kiến Thức
Để hiểu rõ hơn, chúng ta cùng xem xét hai bài tập minh họa từ nội dung bài học.
Bài tập 1: Hợp chất nào dưới đây tạo được liên kết hydro liên phân tử?
Các hợp chất: CH₄, H₂S, HCl, H₂O.
– Phân tích: Nhớ lại điều kiện: nguyên tử H phải liên kết với nguyên tử có độ âm điện lớn (F, O, N). Trong 4 chất trên, chỉ có H₂O thỏa mãn (H liên kết với O).
– Đáp án: H₂O.
Bài tập 2: Biểu diễn liên kết hydro giữa phân tử ethanol (C₂H₅OH) và nước (H₂O).
Giữa hai phân tử này có thể có 4 kiểu liên kết hydro:
1. Nguyên tử H (tích δ+) của nhóm -OH trong ethanol liên kết với nguyên tử O (tích δ-, có cặp electron tự do) của nước.
2. Nguyên tử H (tích δ+) của nhóm -OH trong ethanol này liên kết với nguyên tử O của phân tử ethanol khác (trong trường hợp chỉ có ethanol).
3. Nguyên tử H (tích δ+) của nhóm -OH trong nước liên kết với nguyên tử O của nhóm -OH trong ethanol.
4. Nguyên tử H của phân tử nước này liên kết với nguyên tử O của phân tử nước khác.

Việc nắm vững cách biểu diễn này giúp bạn hình dung rõ ràng cách các phân tử “bắt tay” nhau trong dung dịch. Để rèn luyện thêm kỹ năng phân tích và tính toán trong Hóa học, bạn có thể tham khảo các bài viết về So Sánh Số Thập Phân Lớp 5 và Hướng Dẫn Chi Tiết Cách Đổi Đơn Vị Đo Khối Lượng Sang Số Thập Phân, dù thuộc môn Toán nhưng chúng rèn luyện tư duy logic và xử lý số liệu – những kỹ năng nền tảng không thể thiếu cho môn Hóa.
Kết Luận
Liên kết hydro và tương tác Van der Waals, dù là những lực tương tác yếu, lại đóng vai trò then chốt trong việc định hình thế giới tự nhiên. Từ việc giải thích tại sao nước lại có nhiều tính chất kỳ lạ, tại sao băng lại nổi, cho đến việc dự đoán nhiệt độ sôi của các chất, hai loại tương tác này chính là chìa khóa quan trọng. Hiểu về chúng không chỉ giúp bạn chinh phục các bài tập Hóa học mà còn mở ra góc nhìn sâu sắc hơn về những hiện tượng tưởng chừng rất đỗi bình thường xảy ra xung quanh chúng ta mỗi ngày.
