Chào mừng các bạn học sinh quay trở lại với khóa học của chúng tôi. Trong bài học hôm nay, chúng ta sẽ cùng nhau lật mở những trang sử khoa học thú vị, tìm hiểu về sự tiến hóa của mô hình nguyên tử và khái niệm then chốt trong hóa học hiện đại: orbital nguyên tử (obitan). Đây là nền tảng quan trọng để giải thích mọi tính chất của vật chất xung quanh ta.
Hành Trình Kiến Tạo Mô Hình Nguyên Tử
Lịch sử hiểu biết về nguyên tử là một hành trình dài với những bước đột phá vĩ đại. Mọi thứ bắt đầu từ một thí nghiệm mang tính bước ngoặt.
Vào năm 1909, nhà vật lý người New Zealand Ernest Rutherford đã thực hiện thí nghiệm bắn phá lá vàng bằng chùm hạt alpha. Kết quả bất ngờ cho thấy hầu hết các hạt alpha đi xuyên thẳng qua, trong khi một số ít bị bật ngược trở lại. Điều này dẫn đến một khám phá vĩ đại: nguyên tử có cấu trúc rỗng, với khối lượng tập trung chủ yếu ở một hạt nhân mang điện tích dương, rất nhỏ bé ở trung tâm.
Sau đó, vào năm 1913, nhà vật lý người Đan Mạch Niels Bohr đã bổ sung những ý tưởng quan trọng, giải thích sự chuyển động của các electron xung quanh hạt nhân này. Mô hình kết hợp những phát hiện của hai ông được gọi là mô hình nguyên tử Rutherford – Bohr, hay còn gọi là mô hình hành tinh nguyên tử.
Mô Hình Nguyên Tử Rutherford – Bohr: Những Nội Dung Chính
Mô hình này đã đặt nền móng vững chắc với ba luận điểm cốt lõi:
- Khối lượng tập trung ở hạt nhân: Phần lớn khối lượng nguyên tử nằm ở hạt nhân, vì khối lượng của electron rất nhỏ so với proton và neutron.
- Electron chuyển động trên quỹ đạo xác định: Các electron quay xung quanh hạt nhân theo những quỹ đạo tròn hoặc hình bầu dục, tương tự như các hành tinh quay quanh Mặt Trời.
- Năng lượng electron phụ thuộc vào khoảng cách: Năng lượng của electron phụ thuộc vào khoảng cách từ nó đến hạt nhân. Electron càng ở xa hạt nhân thì có năng lượng càng cao.
Theo mô hình này, dù mang điện tích âm, electron không bị hút vào hạt nhân vì lực hút tĩnh điện này được cân bằng bởi lực quán tính ly tâm khi electron chuyển động.
Các electron được sắp xếp thành từng lớp (K, L, M, N…) từ gần hạt nhân ra ngoài. Chúng sẽ được phân bố vào các lớp gần nhân trước. Ví dụ, nguyên tử Nhôm (Al) có 13 electron được sắp xếp trên 3 lớp: lớp K có 2 electron, lớp L có 8 electron và lớp ngoài cùng M có 3 electron. Số electron tối đa trong mỗi lớp được tính bằng công thức 2n², với n là số thứ tự của lớp (n ≤ 4).

Mô hình Rutherford-Bohr đã giải thích được nhiều hiện tượng, nhưng vẫn có những hạn chế. Nó không đủ để giải thích nhiều tính chất phức tạp của nguyên tử và phân tử. Điều này mở đường cho một cuộc cách mạng tư duy mới.
Sự Ra Đời Của Mô Hình Hiện Đại Và Khái Niệm Orbital
Cùng với sự phát triển mạnh mẽ của cơ học lượng tử, mô hình hiện đại về nguyên tử ra đời, được đề xuất bởi Erwin Schrödinger. Sự khác biệt cơ bản so với mô hình hành tinh là:
Các electron chuyển động rất nhanh xung quanh hạt nhân KHÔNG theo những quỹ đạo xác định. Thay vào đó, người ta chỉ có thể xác định được vùng không gian xung quanh hạt nhân mà xác suất tìm thấy electron là lớn nhất (khoảng 90%). Vùng không gian này được gọi là orbital nguyên tử (obitan) và thường được hình dung như một đám mây electron.

Orbital nguyên tử (kí hiệu là AO) chính là khái niệm then chốt xuất phát từ mô hình hiện đại này. Ví dụ, vùng không gian hình cầu xung quanh hạt nhân nguyên tử Hydro mà xác suất tìm thấy electron ở đó là khoảng 90% chính là orbital của nguyên tử Hydro.
Phân Loại Và Đặc Điểm Của Các Orbital
Khi chuyển động trong nguyên tử, các electron có những mức năng lượng khác nhau. Dựa trên sự khác nhau về hình dạng và sự định hướng của orbital trong không gian, người ta phân loại chúng thành:
- Orbital s: Có dạng hình cầu.
- Orbital p: Có hình số 8 nổi (giống như hai quả bóng dính vào nhau), và tùy thuộc vào định hướng trong không gian mà chia thành px, py, pz.
- Orbital d và f: Có hình dạng phức tạp hơn.

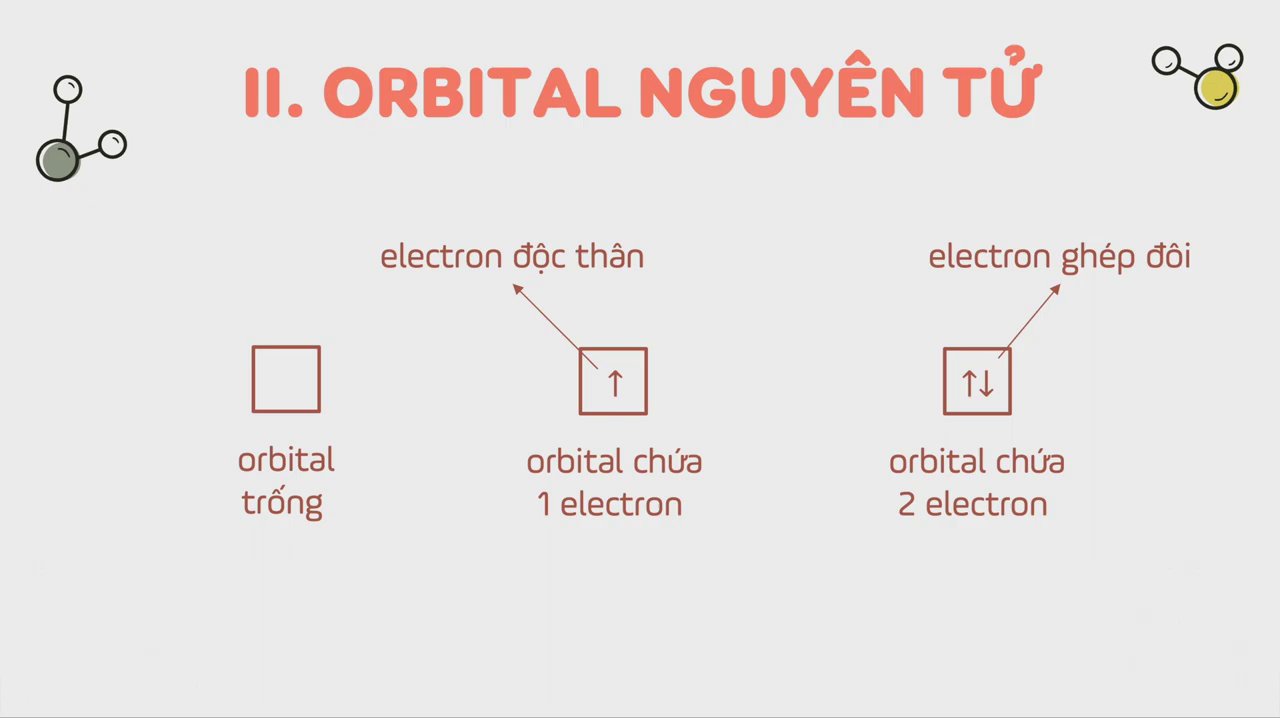
Các orbital có thể được biểu diễn bằng những ô vuông, với các mũi tên đại diện cho electron. Một orbital có thể ở các trạng thái:
– Orbital trống: Không chứa electron.
– Electron độc thân: Orbital chỉ chứa 1 electron.
– Electron ghép đôi: Một orbital chỉ chứa tối đa 2 electron, và cặp electron này được gọi là electron ghép đôi.
Việc nắm vững cách phân bố electron vào các orbital là chìa khóa để hiểu tính chất hóa học của nguyên tố, tương tự như việc thành thạo các phép tính với số thập phân là nền tảng để giải quyết các bài toán phức tạp hơn.
Kết Luận: Từ Mô Hình Cổ Điển Đến Tư Duy Lượng Tử
Bài học hôm nay đã đưa chúng ta đi qua chặng đường phát triển của tư duy về nguyên tử:
- Mô hình Rutherford-Bohr với hình ảnh electron chuyển động trên quỹ đạo như hành tinh.
- Mô hình hiện đại dựa trên cơ học lượng tử, thay thế “quỹ đạo” bằng khái niệm “orbital” – vùng không gian xác suất tìm thấy electron.
- Orbital nguyên tử có các hình dạng đặc trưng (s, p, d, f) và mỗi orbital chỉ chứa tối đa 2 electron.
Sự chuyển đổi từ mô hình hành tinh sang mô hình đám mây electron không chỉ là một bước nhảy vọt về khoa học, mà còn là minh chứng cho sự tiến hóa không ngừng của nhận thức con người. Hiểu rõ điều này chính là chìa khóa để khám phá thế giới vi mô đầy bí ẩn, cũng như việc nắm vững các đơn vị đo lường giúp chúng ta mô tả chính xác thế giới vĩ mô.

Hy vọng bài viết đã giúp bạn có cái nhìn rõ ràng và hệ thống về chủ đề quan trọng này. Hãy cùng luyện tập thêm qua các bài tập để thành thạo kiến thức nhé!
