Định luật tuần hoàn các nguyên tố hóa học không chỉ là một kiến thức nền tảng mà còn là chìa khóa để hiểu và dự đoán tính chất của các chất. Bài viết này sẽ cùng bạn đi từ cơ sở lý thuyết đến các bài tập vận dụng, giúp bạn nắm vững ý nghĩa sâu sắc của bảng tuần hoàn.

Định Luật Tuần Hoàn Các Nguyên Tố Hóa Học: Bản Chất Từ Cấu Hình Electron
Định luật tuần hoàn được phát biểu như sau: Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất, biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
Sở dĩ có sự biến đổi tuần hoàn này là do cấu hình electron, đặc biệt là cấu hình electron lớp ngoài cùng, biến đổi một cách tuần hoàn. Chính sự biến đổi tuần hoàn của cấu hình electron này dẫn đến sự biến đổi tuần hoàn về tính chất của các nguyên tố.
Ví dụ minh họa:
– Ở chu kỳ 2, cấu hình electron lớp ngoài cùng biến đổi từ 2s¹ (Li) đến 2s²2p⁶ (Ne).
– Ở chu kỳ 3, nó lặp lại mô hình tương tự: từ 3s¹ (Na) đến 3s²3p⁶ (Ar).
– Sang chu kỳ 4, mô hình này tiếp tục được lặp lại với sự xuất hiện của phân lớp d.

Ý Nghĩa Của Bảng Tuần Hoàn Trong Dự Đoán Tính Chất
Từ vị trí của một nguyên tố trong bảng tuần hoàn, chúng ta có thể dự đoán được tính chất của đơn chất và hợp chất tạo nên từ nguyên tố đó. Đây là ứng dụng vô cùng quan trọng.
1. So Sánh Tính Phi Kim Trong Cùng Một Nhóm
Xét vị trí của các nguyên tố Clo (Cl), Brom (Br) và Iot (I) trong nhóm VIIA. Trong một nhóm, từ trên xuống dưới, tính phi kim giảm dần. Do đó, ta có thể rút ra kết luận: tính phi kim của Clo mạnh hơn Brom, và Brom mạnh hơn Iot.
Từ tính chất “halogen mạnh đẩy halogen yếu hơn ra khỏi muối của nó”, ta có thể dự đoán phản ứng xảy ra hay không.
– Phản ứng 1: Cho Cl₂ tác dụng với NaBr. Vì Cl mạnh hơn Br, nó có thể đẩy Br ra khỏi muối. Phản ứng xảy ra: Cl₂ + 2NaBr -> 2NaCl + Br₂.
– Phản ứng 2: Cho Br₂ tác dụng với NaCl. Vì Br yếu hơn Cl (hay Cl mạnh hơn Br), Br không thể đẩy Cl ra khỏi muối. Vậy phản ứng này không xảy ra.
2. Dự Đoán Công Thức Oxit Cao Nhất Và Tính Chất
Cho nguyên tố X có số hiệu nguyên tử Z=38. Hãy viết công thức oxit cao nhất và dự đoán oxit này có tính bazơ mạnh hay yếu.
Để làm được, ta cần xác định vị trí của X trong bảng tuần hoàn thông qua cấu hình electron.
– Cấu hình electron của X (Z=38): 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁶ 5s².
– Nguyên tố có 5 lớp electron → thuộc chu kỳ 5.
– Lớp ngoài cùng có 2 electron (5s²) → thuộc nhóm IIA.
– Nguyên tố nhóm IIA có hóa trị cao nhất là II.
– Công thức oxit cao nhất: XO (vì X hóa trị II, O hóa trị II).
– Vì X thuộc nhóm IIA (kim loại kiềm thổ) nên oxit cao nhất của nó có tính bazơ mạnh.

Bài Tập Vận Dụng Định Luật Tuần Hoàn
Bài 1: Xác Định Tính Chất Nguyên Tố
Nguyên tố X có Z=30, cấu hình electron lớp ngoài cùng là 4s² 4p⁶ 4d¹⁰ 5s².
– Vị trí trong bảng tuần hoàn: Z=30 → Số thứ tự 30. Có 5 lớp electron → Chu kỳ 5. Lớp ngoài cùng có 2 electron → Nhóm IIB.
– Tính chất hóa học cơ bản: X thuộc nhóm IIB (kim loại chuyển tiếp) nên có tính kim loại.
– Công thức oxit cao nhất và hidroxit: Thuộc nhóm IIB, hóa trị cao nhất thường là II. Công thức oxit cao nhất có thể là XO, và hidroxit tương ứng là X(OH)₂.
– Phương trình với SO₂: X là kim loại, SO₂ là oxit axit. Kim loại tác dụng với oxit axit có thể tạo ra muối. Ví dụ: 2X + SO₂ -> X₂S + O₂ (tùy điều kiện).
Bài 2: Quy Luật Biến Đổi Tính Chất
Trình bày quy luật biến đổi bán kính nguyên tử, độ âm điện, tính kim loại, tính phi kim của các nguyên tố trong một chu kỳ và trong một nhóm A.
– Trong một chu kỳ (từ trái sang phải):
– Bán kính nguyên tử giảm.
– Độ âm điện tăng.
– Tính kim loại giảm.
– Tính phi kim tăng.
– Trong một nhóm A (từ trên xuống dưới):
– Bán kính nguyên tử tăng.
– Độ âm điện giảm.
– Tính kim loại tăng.
– Tính phi kim giảm.
Bài 3: Dự Đoán Nhóm Nguyên Tố Dựa Vào Phản Ứng
Hidroxit của nguyên tố R có tính bazơ mạnh và tác dụng được với H₂SO₄ theo tỉ lệ mol R(OH)ₓ : H₂SO₄ = 1:1. Dự đoán R thuộc nhóm nào?
– Hidroxit có tính bazơ mạnh → R thuộc nhóm IA hoặc IIA.
– Nếu R thuộc nhóm IA: ROH + H₂SO₄ → RHSO₄ + H₂O. Tỉ lệ mol ROH : H₂SO₄ = 1:1. (Phù hợp với đề bài 1:1).
– Nếu R thuộc nhóm IIA: R(OH)₂ + H₂SO₄ → RSO₄ + 2H₂O. Tỉ lệ mol R(OH)₂ : H₂SO₄ = 1:1. (Cũng phù hợp).
– Kết luận: Dựa vào tỉ lệ 1:1, R có thể thuộc nhóm IA (nếu hóa trị I) hoặc IIA (nếu hóa trị II). Cần thêm dữ kiện để xác định chính xác. Việc lập và cân bằng phương trình hóa học chính xác là kỹ năng nền tảng, tương tự như khi bạn học về tỷ số trong các bài toán thực tế, đòi hỏi sự tỉ mỉ và logic.

Bài 4: Phân Tích Oxit Cao Nhất
Oxit cao nhất của hai nguyên tố S và E khi tan trong nước tạo dung dịch làm quỳ tím chuyển xanh.
– Câu a: Dự đoán S, E thuộc loại nguyên tố nào?
– Oxit tan trong nước tạo dung dịch làm quỳ tím chuyển xanh → Dung dịch có tính bazơ.
– Oxit có tính bazơ mạnh thường là oxit của kim loại kiềm hoặc kiềm thổ.
– → S và E là kim loại, thuộc nhóm IA hoặc IIA.
– Câu b: Dự đoán S và E cùng một chu kỳ hay cùng một nhóm? Giải thích.
– Đề bài cho tỉ lệ nguyên tử S : O và E : O trong các oxit cao nhất là bằng nhau.
– Giả sử chúng cùng nhóm IA, công thức oxit cao nhất là S₂O và E₂O. Tỉ lệ S:O = 2:1, E:O = 2:1 → Bằng nhau.
– Giả sử cùng nhóm IIA, công thức là SO và EO. Tỉ lệ S:O = 1:1, E:O = 1:1 → Cũng bằng nhau.
– Kết luận: Tỉ lệ nguyên tử của chúng với O trong oxit cao nhất bằng nhau nên S và E phải cùng một nhóm.
– Câu c: So sánh số hiệu nguyên tử của S và E. Biết khối lượng phân tử oxit cao nhất của E lớn hơn của S.
– Vì S và E cùng nhóm, công thức oxit cùng dạng (R₂O hoặc RO).
– Khối lượng phân tử E₂O > S₂O (hoặc EO > SO) → Khối lượng nguyên tử của E > Khối lượng nguyên tử của S.
– Trong cùng một nhóm, từ trên xuống dưới, khối lượng nguyên tử tăng dần.
– → Số hiệu nguyên tử của E lớn hơn số hiệu nguyên tử của S.
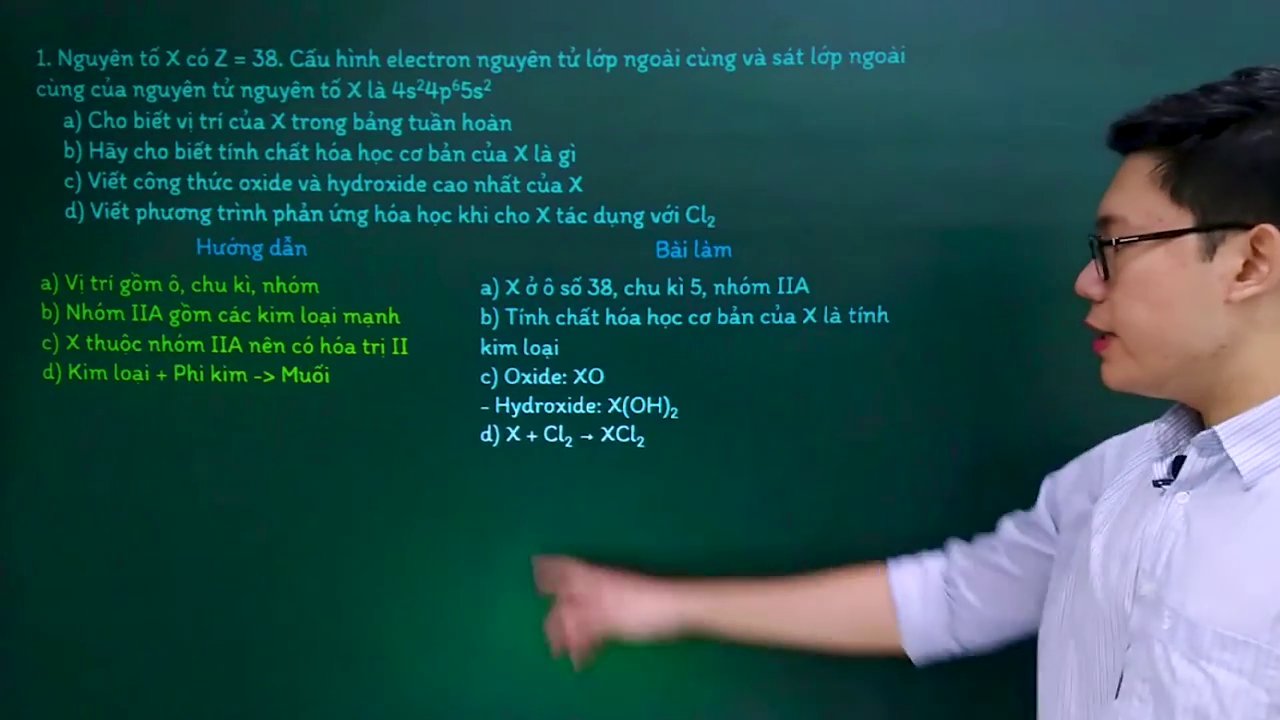
Kết Luận
Định luật tuần hoàn và bảng tuần hoàn các nguyên tố hóa học thực sự là một hệ thống hoàn chỉnh và logic. Nó không chỉ giúp chúng ta sắp xếp các nguyên tố một cách khoa học mà còn là công cụ đắc lực để dự đoán, so sánh tính chất và khả năng phản ứng của chúng. Từ việc nắm vững cơ sở là sự biến đổi tuần hoàn của cấu hình electron, đến việc thành thạo các quy luật biến đổi trong chu kỳ, nhóm, bạn hoàn toàn có thể giải quyết linh hoạt nhiều dạng bài tập từ cơ bản đến nâng cao. Việc học thuộc lòng bảng tuần hoàn sẽ trở nên dễ dàng và có ý nghĩa hơn khi bạn hiểu được những quy luật tiềm ẩn đằng sau nó, giống như việc hiểu bản chất sẽ giúp bạn so sánh và ứng dụng các con số một cách chính xác trong toán học. Hãy coi bảng tuần hoàn như một tấm bản đồ quý giá, dẫn lối bạn khám phá thế giới kỳ diệu của hóa học.
